质量优势
“好的、结构确定的蛋白产品,能够尽可能降低药物研发的不确定性,降低药物研发的每一步风险。”
苗景赟
百普赛斯集团 - 副总裁
RUO级别产品
作为在靶点蛋白开发积累多年开发经验的ACROBiosystems百普赛斯,已经总结出药物开发用靶点蛋白的关键点。
药物开发用靶点蛋白的关键点,主要涵盖五个方面的要素:
纯度和均一性
ACROBiosystems百普赛斯常用的纯度检测方法有SDS-PAGE,HPLC,MALS等。
SDS-PAGE(SDS聚丙烯酰胺凝胶电泳方法),属于变性蛋白分析检测技术,多用于检测目标蛋白和杂蛋白的比例和含量,一般较难看出蛋白在溶液中的聚集情况。
HPLC(高效液相色谱)是蛋白在非变性的状态下、测定溶液中蛋白的纯度和分子量。 MALS(多角度激光散射)是一种先进的蛋白质分子量测定技术,用于检测蛋白在非变性的状态下,溶液中蛋白的分子量和聚集状态。MALS常常和HPLC进行联用,成为常规HPLC技术的有力的补充,可以通过激光散射强度直接测定溶液中蛋白的绝对分子量,且分子量测定不依赖于洗脱体积或保留时间,可以真实测定蛋白在非变性状态下的分子量和聚集状态。使用MALS技术进行质量控制,可以有效保证蛋白的正确天然聚集状态和构象,这是常规HPLC技术所不能实现的。
纯度经MALS验证是ACROBiosystems百普赛斯的优势可以确保蛋白的结构正确,蛋白聚集状态可控产品均一性好,批间一致,这也是ELISA、SPR、BLI活性验证结果一致的基础。所以,对于生物药物开发的客户,所用蛋白的聚集状态,批间差异等都是非常关键的。
ACROBiosystems百普赛斯致力于帮助客户降低药物研发的风险,在纯度方面替客户把好关,为客户提供纯度和均一性好、批间一致,更重要的是结构正确的高质量重组蛋白。
靶点蛋白尽可能地接近天然的构象
因为蛋白结构是功能活性的基础,只有接近天然构象,蛋白才能正确发挥生物学功能。尤其是蛋白天然的聚集存在形式,正确配对二硫键等,这些对于维持蛋白正确结构非常关键,在靶点蛋白开发过程中要重点关注。ACROBiosystems百普赛斯选用HEK293作为宿主细胞的表达系统,由HEK293系统表达的蛋白会得到更充分的修饰,比如糖基化修饰,更接近人体内的天然构象。这是原核表达系统、非人源的真核系统所不能实现的。靶点蛋白作为抗体药开发的关键原料,天然构象、正确结构的高质量靶点蛋白,对于客户免疫获得抗体、筛选功能抗体、临床验证抗体效果等关键应用场景,会显著提高抗体药物开发的成功率,降低药物开发的不确定性。
活性性能经过目标应用场景验证
在靶点蛋白开发过程中会经常遇到同一个蛋白产品在不同应用场景中表现完全不同的情况,因此需要在研发开始前确定研发目标,明确蛋白的目标应用场景。ACROBiosystems百普赛斯蛋白在开发过程中都会把蛋白放在目标应用场景中,尽量模拟客户的应用场景去评估。
产品的批间一致性
ACROBiosystems百普赛斯产品具有高批间一致性,要求对蛋白的生产工艺进行严格的控制,同时建立完善的质量体系,确保产品批间高度一致。
生产的能力和产品持续开发的能力
保证蛋白产品可以长期稳定地生产,保持品质稳定,支持生物药物的研发过程和整个生命周期对蛋白的长期需求。ACROBiosystems百普赛斯拥有超200的专业产品研发人员,新产品开发能力得以充分的保障。
GMP级别产品
ACROBiosystems百普赛斯深入解读国内外相关法规要求,针对细胞治疗药物开发中可能遇到的关键试剂相关问题制定了解决方案。
ACROBiosystems百普赛斯根据中外法规以及客户要求总结了细胞治疗使用GMP级别原材料选择的关键点,并以此为来指导产品的开发、生产和质控
——
您所关心的, 正是我们所关注的。
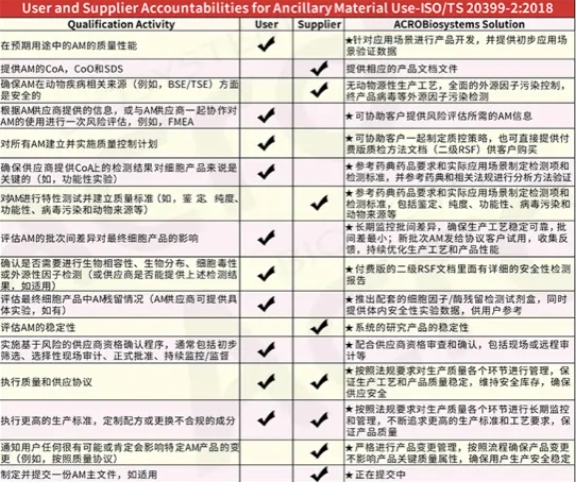
供应商生产资质
● 供应商应通过ISO质量体系认证,具有健全的质量管理体系。
● 生产车间等硬件设施严格符合GMP法规要求(提供第三方权威机构的审计证明,比如药品生产许可证、知名第三方机构的GMP审计报告,其他资质证明文件等)。
● 研发和生产技术先进,具备良好的生产工艺和技术水平,和持续生产供应的能力。
产品质量和性能
● 产品关键质量属性明确,按照药典要求进行全面分析检定和表征:包括鉴别、含量,纯度、生物学活性、水分,工艺相关杂质,潜在污染物等。
● 产品经过实际应用场景充分验证,性能可满足应用要求(如T细胞培养和激活实验)。
● 各分析方法经过系统验证和溯源,准确可靠可重复,能准确的进行产品质量分析检定,以及用于生产批间差长期监控。
● 分析数据完整性符合法规要求。
批间一致性,稳定性
● 生产原料,厂房设备,实验室分析检测,产品包装储存等各方面符合GMP质量管理体系和细胞治疗原辅料的法规要求。
● 生产关键参数控制严格,生产工艺稳定可靠。
● 持续进行生产批间差监控和分析,OOS偏差分析和持续改进,确保产品的生产过程稳定性和批间-致性。
● 产品稳定性充分研究,确保运输、保存和使用过程中,性能稳定可靠。
产品安全性
● 无菌,细菌内毒素,病毒,支原体,相关杂质含量(HCP, DNA,抗生素),终产品残留,其他杂质(异物,添加剂等)
完善的法规支持文档
● 重点关注安全性,包括来源证明、检验报告书(COA) 、委外检测报告和相关资质证明、包装说明书、无TSE/BSE声明、AOF无动物源性声明、DMF文档、RSF法规支持文件等